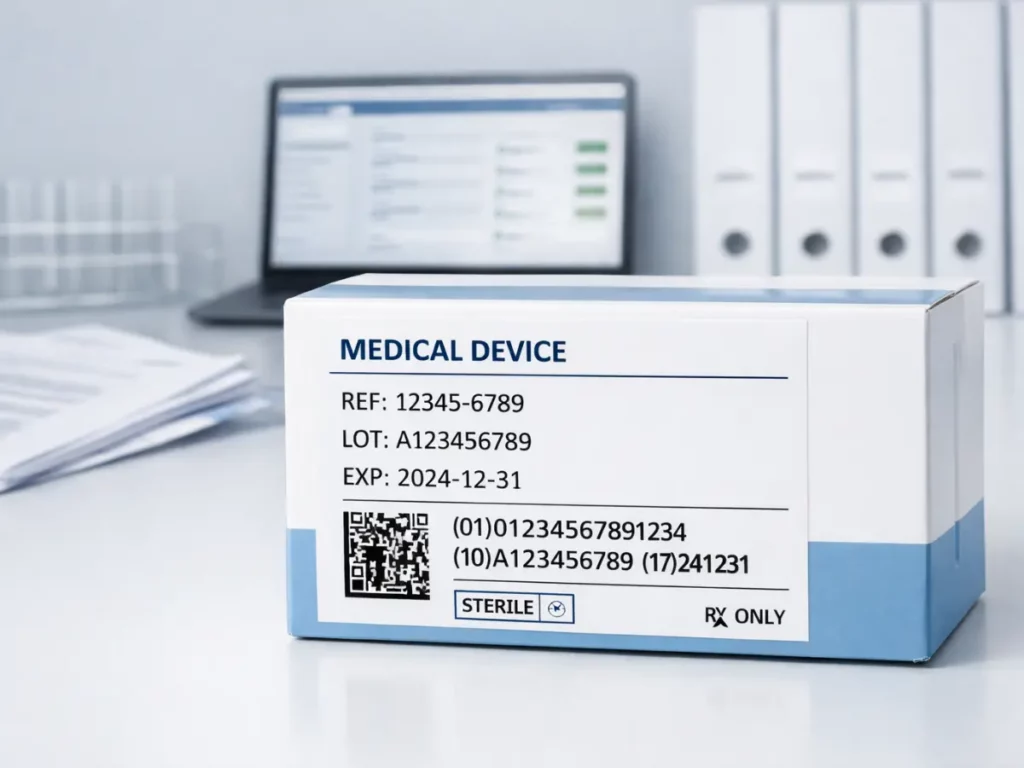
Tracciabilità dei Dispositivi Medici: Cos’è l’UDI e come si usa in Svizzera
La tracciabilità dei dispositivi medici rappresenta oggi uno degli elementi centrali della conformità regolatoria in Svizzera. Con l’entrata in vigore della nuova normativa svizzera allineata al quadro europeo, il sistema UDI (Unique Device Identification) è diventato uno strumento obbligatorio per garantire identificazione univoca, sicurezza del paziente e sorveglianza post-commercializzazione. Per aziende produttrici, fabbricanti e importatori […]
Tracciabilità dei Dispositivi Medici: Cos’è l’UDI e come si usa in Svizzera Leggi tutto »